Перейти к:
Роль реабилитации в развитии моторных навыков у пациентов со спинальной мышечной атрофией 5q, получающих патогенетическую терапию
https://doi.org/10.46563/2686-8997-2025-6-4-209-220
EDN: glkqnk
Аннотация
Введение. Спинальная мышечная атрофия 5q (СМА) — прогрессирующее нейромышечное заболевание, обусловленное мутацией в гене SNN1. Патогенетическая терапия существенно изменила естественное течение заболевания, но не обеспечила полного восстановления ранее утраченных моторных функций. На фоне сохраняющейся мышечной слабости реабилитация остаётся важнейшим компонентом комплексного ведения пациентов. Цель исследования — оценить объём и структуру реабилитации у пациентов со СМА 1–3-го типов, получающих патогенетическую терапию, и определить её связь с динамикой моторного развития по числу моторных навыков.
Материалы и методы. В исследование включено 143 пациента со СМА 1–3-го типов (59 — СМА 1-го типа; 52 — СМА 2-го типа; 32 — СМА 3-го типа) в возрасте 0–18 лет. Медиана времени до начала патогенетической терапии от дебюта заболевания равнялась 6,0 [3,0; 13,0] мес при СМА 1-го типа, 45,0 [14,0; 90,0] мес при СМА 2-го типа и 100,0 [67,0; 147,5] мес при СМА 3-го типа. Период наблюдения составил 3 года от инициации патогенетической терапии. Функциональный статус оценивали по 8 моторным навыкам согласно критериям ВОЗ. Объём реабилитации определяли по опросу и медицинской документации.
Результаты. На фоне патогенетической терапии у пациентов со СМА 1-го типа отмечена положительная динамика развития к конечной точке наблюдения: удержание головы увеличилось с 35,6% случаев до 82,5%, перевороты — с 1,7% до 67,5%, самостоятельное сидение достигнуто у 75% детей, у 15% появилась опора на ноги. У пациентов со СМА 2-го типа на патогенетической терапии зафиксирована стабилизация базовых функций и умеренный прирост сложных моторных навыков (освоение ползания увеличилось с 12,5% до 17,4% пациентов; стояния с поддержкой — с 8,3% до 21,7%; ходьбы с поддержкой — с 2,1% до 13%; самостоятельной ходьбы — до 7,9%). В группе пациентов со СМА 3-го типа моторная динамика на фоне патогенетической терапии характеризовалась преимущественно сохранением имеющихся навыков с отдельными улучшениями (например, рост частоты ползания до 42,9% и единичный случай появления самостоятельной ходьбы у исходно «сидячего» пациента). У исходно «ходячих» пациентов со СМА 3-го типа отмечалась стабилизация состояния. Выявлена значимая связь между числом приобретённых моторных навыков и объёмом реабилитации у пациентов со СМА 1-го типа, а также у исходно «сидячих» пациентов со СМА 2-го и 3-го типов (p ≤ 0,014). У пациентов со СМА 1-го типа регулярная комплексная реабилитация обеспечивала достоверно более высокие показатели моторных навыков по сравнению со всеми другими подходами (ppadj < 0,001). У пациентов со СМА 2-го типа регулярные формы реабилитации (комплексная или домашняя) демонстрировали преимущество перед курсовой реабилитацией (ppadj ≤ 0,024). В группе со СМА 3-го типа у сидячих пациентов реабилитация курсами (курсовая) в течение года приводила к лучшему моторному ответу на лечение по сравнению с детьми, не получающими реабилитации (ppadj = 0,028).
Заключение. Реабилитационные мероприятия на регулярной основе, особенно в комплексе с курсами на базе медицинских центров, были связаны с лучшим моторным ответом на патогенетическую терапию как у пациентов со СМА 1-го типа, так и у исходно «сидячих» пациентов со СМА 2-го и 3-го типов. Полученные данные подтверждают важную роль непрерывной реабилитации в составе стандарта ведения пациента со СМА как необходимого условия достижения наилучшего моторного прогресса при современных терапевтических патогенетических подходах.
Соблюдение этических стандартов. Исследование одобрено локальным этическим комитетом РНИМУ им. Пирогова (протокол № 226 от 20.02.2023).
Участие авторов:
Папина Ю.О. — обзор публикаций по теме статьи, сбор и анализ данных, написание текста статьи, формулирование выводов;
Стеванович А.Р. — обзор публикаций по теме статьи, написание текста статьи;
Мельник Е.А. — редактирование статьи, формулирование выводов;
Артемьева С.Б. — координация исследования;
Влодавец Д.В. — координация исследования, редактирование статьи.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Исследование не имело спонсорской поддержки.
Поступила 03.11.2025
Принята к печати 01.12.2025
Опубликована 31.01.2026
Для цитирования:
Папина Ю.О., Стеванович А.Р., Мельник Е.А., Артемьева С.Б., Влодавец Д.В. Роль реабилитации в развитии моторных навыков у пациентов со спинальной мышечной атрофией 5q, получающих патогенетическую терапию. Неврологический журнал имени Л.О. Бадаляна. 2025;6(4):209-220. https://doi.org/10.46563/2686-8997-2025-6-4-209-220. EDN: glkqnk
For citation:
Papina Yu.O., Stevanovich A.R., Melnik E.A., Artemyeva S.B., Vlodavets D.V. The role of rehabilitation in the development of motor skills in patients with spinal muscular atrophy 5q receiving pathogenetic therapy. L.O. Badalyan Neurological Journal. 2025;6(4):209-220. (In Russ.) https://doi.org/10.46563/2686-8997-2025-6-4-209-220. EDN: glkqnk
Введение
Спинальная мышечная атрофия (СМА) — тяжёлое аутосомно-рецессивное нейродегенеративное заболевание, приводящее к дефициту полноценного белка SMN, прогрессирующей гибели мотонейронов спинного мозга и вялому параличу [1–3]. Традиционно заболевание подразделяют на 1–3-й типы в зависимости от возраста манифестации и максимальных двигательных возможностей пациента [4–6].
Внедрение патогенетической терапии (нусинерсен, рисдиплам, онасемноген абепарвовек МНН) кардинально изменило естественное течение СМА, замедлив прогрессирование вторичных осложнений и создав условия для сохранения и развития моторных функций [6–16]. В этой новой парадигме систематическая реабилитация перестала быть паллиативной мерой, превратившись в обязательный компонент лечения, улучшающий эффект фармакотерапии и направленный на максимальную реализацию функционального потенциала пациентов [17–25].
Физиологическое обоснование необходимости реабилитации многогранно. Во-первых, дозированная физическая активность способна стимулировать нейропластичность и поддерживать мышечную массу, что особенно важно на фоне патогенетического лечения [22, 26]. Во-вторых, реабилитация является ключевым методом профилактики вторичных осложнений: контрактур суставов, сколиоза, дыхательной недостаточности, связанной с деформацией позвоночника, которые сами по себе ухудшают качество жизни и ограничивают мобильность пациентов [27].
Современная реабилитация при СМА — гибкая система мероприятий, направленная на замедление осложнений и раскрытие функционального потенциала каждого пациента [17, 18, 20, 25, 28–31]. Основные подходы к реабилитации пациентов со СМА отражены в действующих клинических рекомендациях [4, 5].
Эффективность реабилитации при СМА достигается, если она соответствует следующим принципам (принципы эффективной реабилитации):
- раннее начало реабилитации — с момента постановки диагноза или проявления первых симптомов;
- мультидисциплинарность — сочетание консультации профильных врачей, лечебной физкультуры (ЛФК), эрготерапии, использования технических средств реабилитации (ТСР), логопедии, ортезирования и психологической поддержки;
- индивидуализация — в соответствии с актуальным состоянием пациента и регулярная переоценка;
- непрерывность — внедрение комплекса ежедневной домашней реабилитации в привычный режим дня пациента;
- фокус на качестве жизни и максимальной самостоятельности пациента.
Несмотря на доказанную важность комплексной реабилитации, в реальной клинической практике сохраняется значительный разрыв между рекомендациями и фактическим объёмом получаемой пациентами реабилитационной помощи. Исследования указывают на то, что на момент начала патогенетического лечения многие пациенты, особенно с тяжёлыми формами СМА, не получали адекватного восстановительного лечения [32]. Основными барьерами являются тяжесть состояния, ограниченная доступность реабилитации и недостаточная информированность и мотивированность родителей, неприверженность медицинским рекомендациям.
Следует учитывать важность проактивного подхода — превентивное начало реабилитации, до момента начала формирования вторичных ортопедических осложнений, предотвратит их формирование (или значительно отсрочит их появление или снизит степень их тяжести), которые могут ограничить функциональные возможности, несмотря на увеличение мышечной силы на фоне патогенетического лечения [33–38].
Ещё одной актуальной задачей является поиск чувствительных инструментов для оценки эффективности реабилитации. Функциональные шкалы, рекомендуемые для оценки эффективности патогенетической терапии (CHOP INTEND, HINE-2, HFMSE, RULM, MFM-32, 6MWT), могут быть недостаточно чувствительны для фиксации минимального прогресса у пациентов с тяжёлыми ограничениями или в состоянии стабилизации, не отражать все имеющиеся навыки и имеют ограничения, связанные с методологией применения, зависят от опыта исследователя [33–35, 37, 39–41]. В этой связи перспективным представляется использование количественных показателей, таких как подсчёт ключевых двигательных умений, что позволяет детализировать динамику даже при отсутствии смены функционального класса (ФК) [42].
Таким образом, в условиях новой терапевтической эры при СМА приобретает первостепенное значение комплексная оценка объёмов, доступности и эффективности реабилитации.
Цель настоящего исследования — проведение оценки объёмов и видов реабилитации, получаемой пациентами с различными типами СМА на фоне патогенетической терапии, и анализ связи между объёмом реабилитации и динамикой моторного развития, оцениваемой по количеству моторных навыков.
Материалы и методы
Критерием включения в исследование был диагноз СМА 5q, подтверждённый молекулярно-генетическими методами, в том числе установленный по результатам расширенного неонатального скрининга в возрасте от 0 до 18 лет. Все дети наблюдались в детском психоневрологическом отделении № 2 Научно-исследовательского клинического института педиатрии и детской хирургии им. акад. Ю.Е. Вельтищева РНИМУ им. Н.И. Пирогова и получали один из видов патогенетического лечения (МНН — онасемноген абепарвовек, рисдиплам, нусинерсен) или была проведена последовательная смена одного вида лечения на другой. Дети на комбинированной терапии не включались в исследование. От всех законных представителей пациентов получено письменное информированное согласие об участии в исследовании. Критерием исключения являлся отказ родителей от участия их ребёнка в исследовании. В работе проводился ретроспективный анализ с серией проспективных наблюдений за период с апреля 2021 г. по декабрь 2024 г.
В исследование включены 143 пациента со СМА 1–3-го типов в возрасте от 0 до 18 лет. Группа со СМА 1-го типа (СМА1) состояла из 59 (41,3%) пациентов, все они относились к ФК «лежачий» на момент включения. В группу со СМА 2-го типа (СМА2) вошли 52 (36,4%) пациента, среди которых 4 (7,7%) ребёнка имели ФК «лежачий», а 48 (92,3%) — «сидячий». Группа со СМА 3-го типа (СМА3) включала 32 (22,4%) пациента, из которых 19 (59,4%) исходно относились к ФК «сидячий» и 13 (40,6%) — к ФК «ходячий».
Гендерный состав был относительно сбалансированным: в группе СМА1 — 28 (47,5%) девочек и 31 (52,5%) мальчик; СМА2 — 29 (55,8%) девочек и 23 (44,2%) мальчика; СМА3 — по 16 (50,0%) девочек и мальчиков. У пациентов группы СМА1 медиана возраста появления симптомов составила 3,0 [1,0; 4,0] мес, СМА2 — 7,5 [6,0; 11,0], СМА3 — 18,0 [12,0; 24,0].
Возраст начала патогенетической терапии существенно различался между фенотипами. У пациентов группы СМА1 медиана начала лечения составила 9,0 [5,0; 18,0] мес, тогда как у пациентов группы СМА2 — 55,0 [22,0; 100,5]. В группе СМА3 старт лечения приходился на ещё более старший возраст, медиана составила 114,0 [83,5; 166,5] мес. Медиана от дебюта заболевания до начала лечения составила в группе СМА1 6,0 [3,0; 13,0] мес, в группе СМА2 — 45,0 [14,0; 90,0], а в группе СМА3 — 100,0 [67,0; 147,5].
Распределение видов терапии существенно различалось между группами. В группе СМА1 онасемноген абепарвовек МНН получили 15 (25,4%) пациентов, рисдиплам МНН — 11 (18,6%), нусинерсен МНН — 15 (25,4%). Переход с нусинерсена на онасемноген абепарвовек был зафиксирован у 10 (16,9%) пациентов, переход с рисдиплама на онасемноген абепарвовек — у 7 (11,9%). Ещё 1 (1,7%) пациент последовательно получил нусинерсен, затем рисдиплам и далее онасемноген абепарвовек. В группе СМА2 нусинерсен получали 19 (36,5%) пациентов, рисдиплам — 16 (30,8%), онасемноген абепарвовек — 10 (20,8%). Последовательная терапия нусинерсеном с переходом на онасемноген абепарвовек была у 5 (9,6%) пациентов, а переход с рисдиплама на онасемноген абепарвовек — у 2 (3,8%). Применение терапии у пациентов в группе СМА3: нусинерсен получали 27 (84,4%) человек, тогда как рисдиплам — 5 (15,6%); онасемноген абепарвовек в этой группе не использовался.
В исследовании использовались условные обозначения визитов:
- визит 0.0 — за 0–3 мес до начала патогенетической терапии;
- визит 1.0 — через 1 год (интервал 9–15 мес);
- визит 2.0 — через 2 года (интервал 21–27 мес);
- визит 3.0 — через 3 года (интервал 33–39 мес).
В рамках оценки эффективности патогенетической терапии (визиты 0.0–3.0) проводилось исследование 6 ключевых моторных навыков (сидение 10 с и более без поддержки, стояние с поддержкой, ползание на четвереньках, стояние без поддержки, ходьба вдоль опоры и самостоятельная ходьба на 5 и более шагов без поддержки) по критериям ВОЗ. Дополнительно оценены навыки удержания головы в вертикальном положении и переворотов. Всем пациентам присваивался ФК в соответствии с предложенными критериями Ю.О. Папиной и соавт. [43].
Объём получаемой пациентами реабилитации оценивали на основании опроса родителей/пациентов, а также согласно медицинским выпискам пациентов из стационаров за год, предшествующий визиту. Все подходы к реабилитации были разделены на 4 группы:
- Полное отсутствие любых видов реабилитации: ребёнок не получал домашнюю реабилитацию (не занимался дома ЛФК, ортопедическими растяжками, не имел возможности дома заниматься на тренажёрах, не посещал бассейн на регулярной основе и др.) и не прошёл 2 и более курсов восстановительного лечения и реабилитации в специализированных медицинских учреждениях в течение года перед визитом.
- Домашняя реабилитация: в течение года перед оценкой ребёнок занимался различными видами восстановительного лечения дома на регулярной основе (не менее 2 раз в неделю) и с применением не менее 3 различных методик (например, ЛФК, массаж, ортопедические растяжки, занятия на тренажёрах или посещение бассейна на регулярной основе и другие методики), использование которых возможно по месту жительства. При этом ребёнок не проходил два и более курсов восстановительного лечения и реабилитации в специализированных учреждениях в течение года перед визитом (курсовую реабилитацию).
- Курсовая реабилитация: ребёнок проходил 2 и более курса восстановительного лечения и реабилитации в специализированных учреждениях длительностью 10-14 дней в течение года перед визитом. При этом он не получал домашнюю реабилитацию в интервале между курсами.
- Комплексная реабилитация: ребёнок регулярно занимался дома, получал домашнюю реабилитацию и дополнительно курсовую реабилитацию 2 и более раза в год перед визитом.
Основным методом, оцениваемым в исследовании, являются нетехнические методы реабилитации. Отдельное применение таких методик, как физиотерапевтическое лечение, электростимуляция, не учитывалось, поскольку их обычно включают в программу комплексной курсовой реабилитации. Не оценивалось использование ТСР, поскольку в данном исследовании не проводилась оценка ортопедических осложнений заболевания и не анализировалась потребность пациентов в креслах-колясках, вертикализаторах и ортопедических изделиях. Число обследованных пациентов в каждой точке могло отличаться в связи с неявкой на визиты и/или отсутствии данных в медицинской документации.
Статистический анализ проведён с применением программного пакета «SPSS Statistics v. 26.0» («IBM»). Нулевую гипотезу отвергали при уровне значимости р < 0,05 (в случае апостериорных попарных сравнений — при скорректированном уровне значимости рadj < 0,05). Количественные переменные описывали с помощью среднего значения и стандартного отклонения и/или медианы и квартилей, дополнительно указывали диапазон значений. Поскольку число моторных навыков имело ненормальное распределение, применяли тест Краскела–Уоллиса с апостериорными попарными сравнениями, для поправки на множественные сравнения применяли метод Бонферрони.
Результаты
Моторные навыки и объём проводимой реабилитации
Все пациенты в группе СМА1 (n = 59) на старте исследования имели ФК «лежачий». До начала патогенетической терапии (визит 0.0) удерживать голову в вертикальном положении могли 21 (35,6%) из 59 детей. К визиту 3.0 этот навык отмечался уже у 33 (82,5%) из 40 пациентов. Число детей, способных выполнять перевороты в обе стороны в положении лежа, возросло с 1 (1,7%) из 59 на старте до 27 (67,5%) из 40 к окончанию наблюдения. На визите 0.0 ни один ребенок не демонстрировал умения сидеть без поддержки 10 и более секунд, однако к визиту 3.0 этот навык сформировался у 30 (75%) из 40 пациентов; 4 (10,0%) из 40 детей освоили ползание на четвереньках, 6 (15,0%) из 40 могли стоять с поддержкой, а 3 (7,5%) из 40 — ходить с поддержкой. Навыков самостоятельного стояния и самостоятельной ходьбы в течение всего периода наблюдения среди пациентов в группе СМА1, получающих патогенетическую терапию, не достигнуто. В итоге, в группе СМА1 75% пациентов из оценённых к третьему году наблюдения достигли ФК «сидячий».
На начальном этапе (визит 0.0) из 59 пациентов, включенных в исследование, данные по реабилитации были доступны для 57 человек. Из них 37 (64,9%) пациентов в группе СМА1 не получали реабилитации, тогда как комплексная реабилитация была представлена лишь у 7 (12,3%). К визиту 3.0 ситуация принципиально изменилась: комплексная реабилитация становилась ведущей формой — у 24 (63,2%) из 38 пациентов, а отсутствие реабилитации встречалось уже только у 3 (7,9%). Фактически у 92,1% пациентов на 3-м году исследования (к визиту 3.0) применялся хотя бы один вид реабилитации. Таким образом, наблюдался выраженный переход от высокой доли отсутствия реабилитации к доминированию комплексной программы реабилитации у пациентов в группе СМА1 (рис. 1).
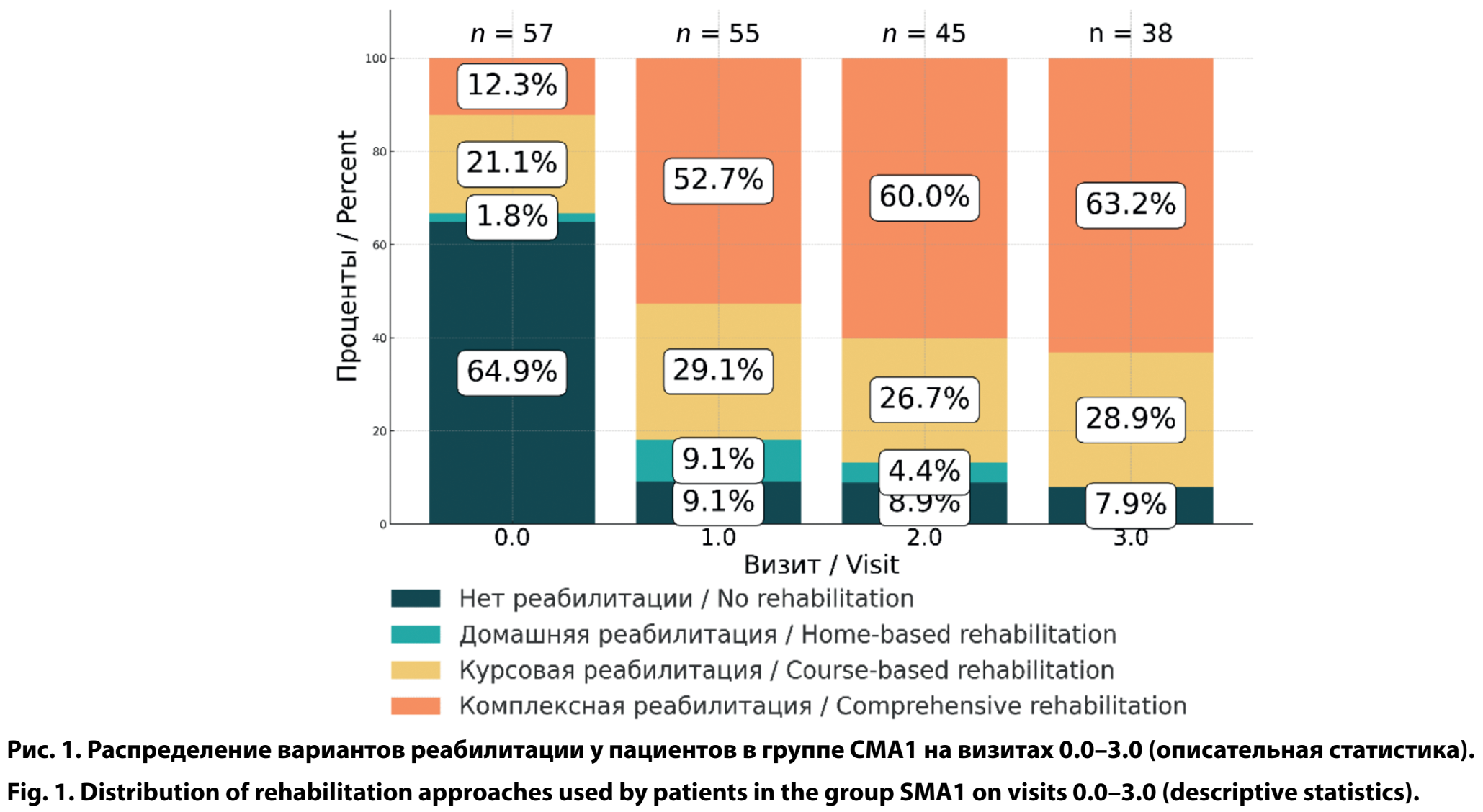
В группе СМА2 на старте исследования (визит 0.0) было 48 пациентов с ФК «сидячий». На всех этапах наблюдения 100% пациентов сохраняли умение удерживать голову и сидеть самостоятельно не менее 10 с. Динамика более сложных моторных функций: частота ползания изменялась с 6/48 (12,5%) до 4/23 (17,4%); стояния с поддержкой — с 4/48 (8,3%) до 5/23 (21,7%); ходьбы с поддержкой — с 1/48 (2,1%) до 3/23 (13,0%). Способность к самостоятельной ходьбе развилась максимально к визиту 2.0 у 3/38 (7,9%) детей, таким образом ими был достигнут ФК «ходячий».
В группе СМА2 у «сидячих» пациентов на первом осмотре (визит 0.0) данные по реабилитации были доступны у 45 пациентов, не получали реабилитацию почти половина — 20 (44,4%). К визиту 3.0 доля таких пациентов снизилась до 4/22 (18,2%). Напротив, комплексная реабилитация, которую на старте получали лишь 4/45 (8,9%), к конечной точке стала наиболее распространённой — 9/22 (40,9%). Домашняя и курсовая формы реабилитации к визиту 3.0 распределялись как 8/22 (36,4%) и 1/22 (4,5%) соответственно. Полная динамика объёма реабилитации у пациентов в группе СМА2 представлена на рис. 2.
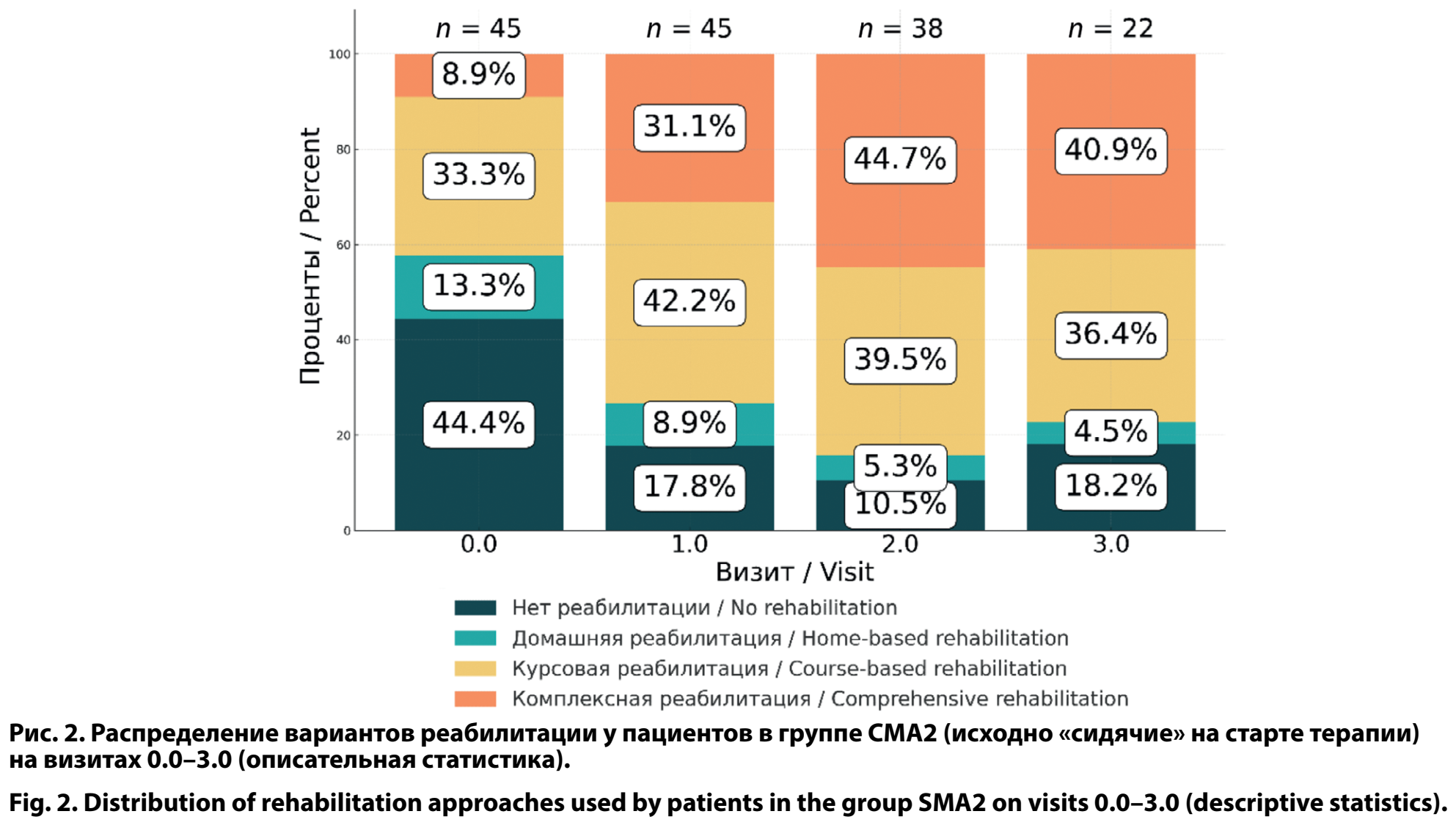
У пациентов в группе СМА3, исходно имевших ФК «сидячий» (n = 19), базовые умения, такие как удержание головы и сидение без опоры, фиксировались у всех детей на всём протяжении наблюдения. Ползание на четвереньках отмечалось у 4/19 (21,1%) на старте и у 3/7 (42,9%) к визиту 3.0; самостоятельная ходьба достигнута лишь у 1/7 (14,3%) ребёнка начиная с визита 1.0.
У исходно «сидячих» пациентов в группе СМА3 на осмотре 0.0 большинство не получали реабилитацию — 13/18 (72,2%). На последующих визитах эта доля оставалась высокой: 10/18 (55,6%) на визите 2.0 и 4/7 (57,1%) — на 3.0. Остальные формы реабилитации встречались значительно реже. Курсовая реабилитация составляла 3/18 (16,7%) на визите 0.0, затем 8/19 (42,1%) на 1.0 и 6/18 (33,3%) на 2.0; к визиту 3.0 её получал лишь 1 (14,3%) ребёнок. Домашняя и комплексная формы во всех точках не превышали 5–14%.
Среди «ходячих» пациентов в группе СМА3 при первом осмотре данные были получены у 11 детей, из которых 5 (45,5%) не получали реабилитации; остальные 18,2% распределялись между домашней, курсовой и комплексной формами. К визиту 3.0 доля детей без реабилитации снизилась до 1/6 (16,7%), а комплексная реабилитация стала ведущей — 4/6 (66,7%). Полная динамика у пациентов в группе СМА3 показана на рис. 3.
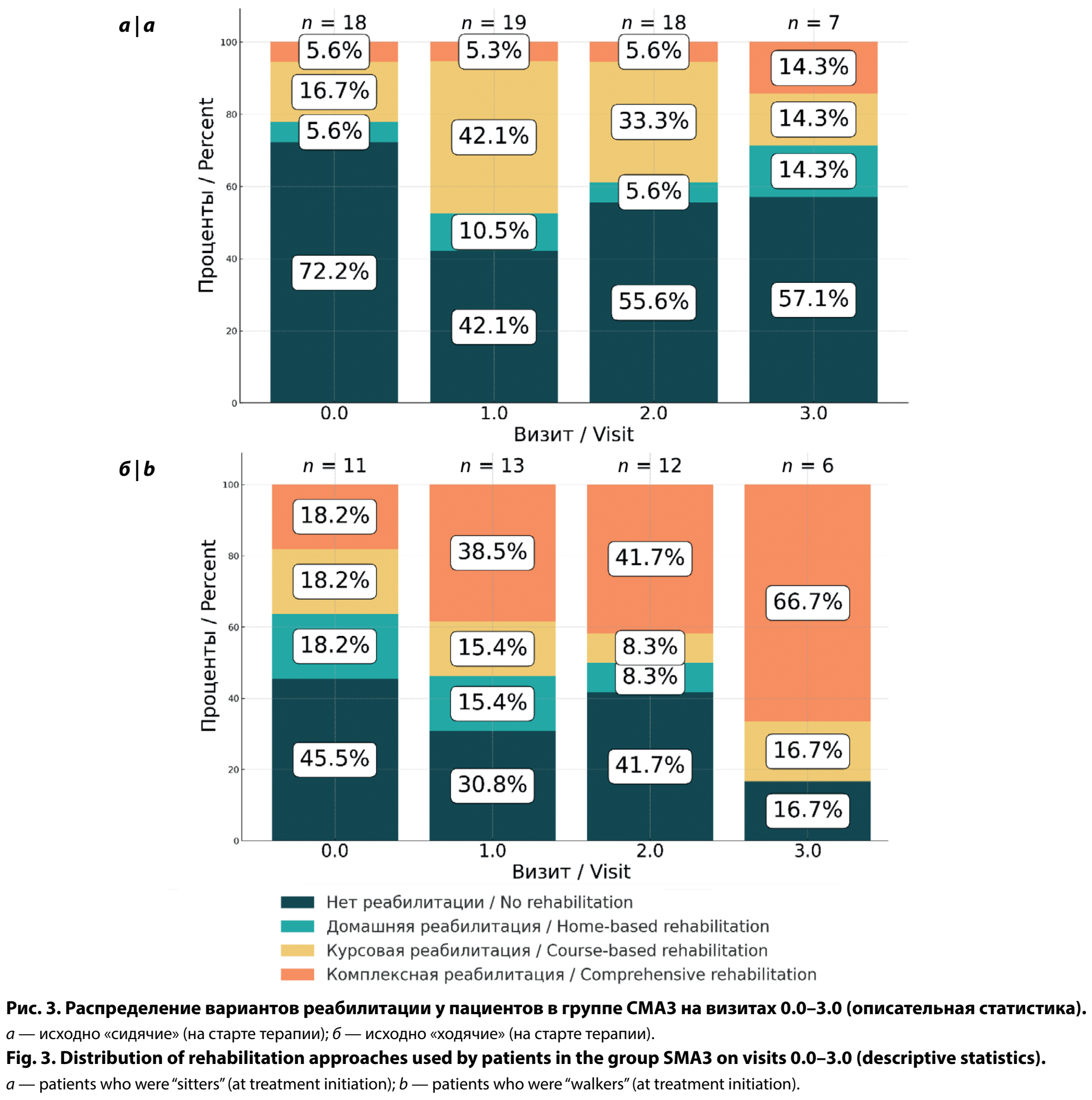
Проведено исследование связи общего числа моторных навыков с объёмом реабилитации за год (таблица). Оценка проводилась, начиная с визита 1.0. При выявлении связи общего числа моторных навыков с объёмом реабилитации за прошедший год единицей наблюдения («случай») считался момент времени, в который были оценены оба показателя. Следовательно, у одного пациента могло быть несколько «случаев», если такая оценка происходила в нескольких временных точках.
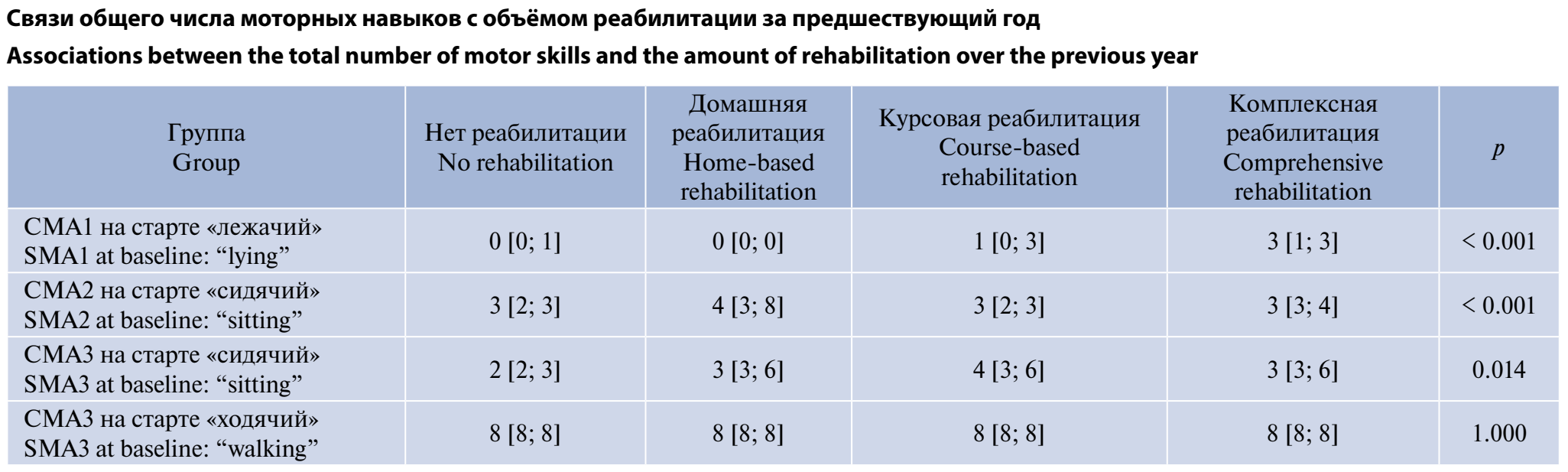
В группе пациентов СМА1 медианное число моторных навыков было различным и существенно и достоверно отличалось для разных объёмов реабилитации: от 0 [0; 1] при отсутствии реабилитации до 3 [1; 3] при применении комплексной реабилитации. Статистический анализ подтвердил значимость этих различий (р < 0,001), причём апостериорные сравнения выявили значимые отличия между комплексной реабилитацией и всеми остальными вариантами реабилитации (рpadj < 0,001).
Для исходно «сидячих» пациентов в группе СМА2 общее число моторных навыков также достоверно различалось в зависимости от формы реабилитации (р < 0,001): медианные значения определены от 3 [2; 3] при отсутствии реабилитации до 4 [3; 8] при домашней реабилитации. Апостериорные сравнения показали значимые отличия между отсутствием реабилитации и комплексной реабилитацией (рpadj = 0,031), а также между курсовой и комплексной реабилитацией (рpadj = 0,007) и между домашней и курсовой реабилитацией в пользу регулярной домашней реабилитации (рpadj = 0,024). Результаты указывают на преимущества регулярных занятий (комплексного или домашнего подхода) перед курсовой реабилитацией.
У пациентов в группе СМА3 исходно с ФК «сидячий» различия по общему числу моторных навыков при разных объёмах реабилитации также были статистически значимыми (р = 0,014) с лучшими результатами при курсовой (медиана 4 [3; 6]) и комплексной (медиана 3 [3; 6]) реабилитации. Апостериорные попарные сравнения выявили значимые различия только между группами полного отсутствия реабилитации и курсовой реабилитации (рpadj = 0,028). Таким образом те, кто реабилитировался хотя бы 2 раза в год курсом, имел большее число моторных навыков, чем те, кто не реабилитировался.
Дополнительно проводился анализ связи улучшения ФК с объёмом реабилитации за предшествующий год. Однако его проведение было сопряжено с рядом ограничений. Анализ показал, что понятие «улучшение ФК» в ряде случаев теряет чувствительность. Представление моторного развития не количественным (число моторных навыков), а категориальным (улучшение ФК — «да»/»нет») показателем требует применения других методов анализа (метод χ2 и точный критерий Фишера), обладающих более низкой чувствительностью. Это приводит к меньшей статистической мощности анализа, что, вероятно, и обусловило отсутствие значимых результатов в подгруппах, где они были получены при анализе общего числа моторных навыков.
Вероятно, именно по этой причине в группе пациентов СМА1 и ФК «лежачий» связь между улучшением ФК и объёмом реабилитации не достигла статистической значимости (р = 0,080), тогда как связь между числом моторных навыков и объёмом реабилитации была значимой (р < 0,001). Аналогично, в группе пациентов СМА3 и ФК «сидячий» связь между улучшением ФК и объёмом реабилитации не достигла статистической значимости (р = 0,500), тогда как связь между общим числом моторных навыков и объёмом реабилитации была значимой (р = 0,014). Лишь в группе СМА2 и ФК «сидячий» на старте с объёмом реабилитации были значимо связаны и число моторных навыков (р < 0,001), и улучшение ФК (смена на более высокий) (р = 0,014).
Для пациентов из группы СМА3 с исходным ФК «ходячий» сравнительный анализ не проводился, поскольку количество моторных навыков на протяжении всего наблюдения оставалось максимальным (n = 8), как и сам ФК.
Подход к исследованию связей объёма реабилитации с функциональными моторными шкалами (CHOP INTEND, HINE-2, HFMSE, RULM и др.) не использовался по причине невозможности статистической обработки в точке перехода с одной шкалы на другую, учитывая методологию применения шкал (смену шкал в зависимости от ФК и возраста пациента).
Обсуждение
Структура включённой выборки существенно определяла ожидаемую динамику моторного ответа. Пациенты со СМА 1-го типа, у которых дебют заболевания приходился на медианный возраст 3 [1,0; 4,0] мес, а лечение начиналось относительно рано — в 9 [5,0; 18,0] мес, демонстрировали наиболее выраженную положительную моторную динамику. Это согласуется с данными литературы, указывающими, что ранний возраст начала терапии и высокая нейропластичность раннего детского возраста создают условия для достижения новых моторных навыков и фенотипической модификации заболевания [44, 45]. У пациентов со СМА 1-го типа в нашем исследовании отмечено существенное улучшение моторных навыков: удержание головы увеличилось с 35,6 до 82,5%, перевороты — с 1,7 до 67,5%, а самостоятельное сидение было достигнуто у 75% детей, что соответствует фенотипическому сдвигу, описанному в систематических обзорах, где достижение новых моторных вех при терапии всеми препаратами для патогенетического лечения СМА наблюдалось у значимой части пациентов со СМА 1-го типа [9, 44, 45].
У пациентов со СМА 2-го типа отмечались значительно более поздний старт терапии (медиана 55 [22,0; 100,5] мес) и длительный период без патогенетического лечения (медиана времени между инициацией терапии и дебютом заболевания — 45 [14,0; 90,0] мес). В соответствии с данными литературы, такие анамнестические характеристики ограничивают потенциал выраженного моторного улучшения, приводя преимущественно к стабилизации базовых двигательных навыков и умеренному приросту сложной моторики [11, 45, 46]. У пациентов со СМА 2-го типа была зафиксирована стабилизация базовых навыков и прирост сложных (ползание — с 12,5 до 17,4%, стояние с поддержкой — с 8,3 до 21,7%, ходьба с поддержкой — с 2,1 до 13%; самостоятельная ходьба — у 7,9%), что согласуется с данными обзоров [11, 44, 45].
Пациенты со СМА 3-го типа характеризовались ещё более поздним началом терапии (медиана 114 [83,5; 166,5] мес) и длительным интервалом между дебютом и лечением (медиана 100 [67,0; 147,5] мес), что отражает хроническое, медленно прогрессирующее течение заболевания до терапевтического вмешательства. Полученная в этой группе динамика моторного развития — преимущественно сохранение существующих навыков с отдельными умеренными улучшениями — соответствует опубликованным данным, где стабилизация (и сохранение амбулаторности для ходячих пациентов) рассматривается как основной ожидаемый результат терапии у поздно леченных пациентов старшего возраста [11, 45, 46].
Таким образом, динамика моторного развития во всех трёх группах совпадает с результатами крупных обзоров и подтверждает фенотипическую эволюцию СМА при применении патогенетических препаратов.
Перед стартом патогенетической терапии значительное количество пациентов не получали никакого вида реабилитации за предшествующий год: в группе СМА1 — 64,9%, в группе СМА2 ФК «сидячий» — 44,4%, в группе СМА3 ФК «сидячий»— 45,5% и в группе СМА3 ФК «ходячий» — 72,2%. Вероятно, такая ситуация связана с основными осложнениями у детей со СМА при естественном течении, особенно у пациентов со СМА 1-го и 2-го типов, такими как: тяжесть состояния ребёнка, обусловленная зависимостью от респираторной поддержки, наличием сколиоза и многочисленных контрактур крупных суставов, доступности реабилитации для тяжёлых пациентов.
Промежуточные осмотры показали колебания в распределении пациентов по видам реабилитации, при этом отмечается тенденция к увеличению доли пациентов, получающих различные виды реабилитации, и снижению доли тех, кто не получает реабилитационные мероприятия.
Во всех группах отмечался переход к более широкому применению комплексной реабилитации. У пациентов в группе СМА1 она стала доминирующим подходом, а в группах СМА2 (исходно «сидячие») и СМА3 (исходно «ходячие») её использование также выросло к визиту 3.0. Это свидетельствует о включении и вовлечении семьи в процесс реабилитации и, вероятно, об улучшении соматического статуса, особенно у тяжёлых пациентов, что позволило чаще получать курсы восстановительного лечения на базе реабилитационных центров или стационаров и улучшило приверженность комплексному и непрерывному подходу со стороны родителей этих пациентов.
Отличия были более выражены в группе СМА3 среди исходно «сидячих» пациентов, где сохранялась тенденция низкой приверженности реабилитации — 57,1% не получали восстановительное лечение к визиту 3.0. Возможно, это связано с недооценкой тяжести заболевания и необходимости реабилитации среди пациентов со СМА 3-го типа, низкой приверженности медицинским рекомендациям со стороны семей и иным.
В настоящем исследовании выявлены связи между числом моторных навыков и объёмом реабилитации у пациентов с различными типами СМА. Так, у пациентов со СМА 1-го типа и исходно «сидячих» со СМА 2-го и 3-го типов медианное число моторных навыков значимо отличалось при различных подходах к реабилитации, наличие реабилитации было связано с более высокой моторной функцией (p ≤ 0,014). У пациентов со СМА 1-го типа апостериорные сравнения показали достоверное преимущество комплексной реабилитации по сравнению со всеми другими вариантами (рpadj < 0,001). У пациентов со СМА 2-го типа выявлены преимущества регулярных занятий (комплексного или домашнего подхода) перед курсовой реабилитацией (рpadj ≤ 0,024). У пациентов со СМА 3-го типа исходно «сидячих» 2 и более курсов реабилитации в год (курсовая реабилитация) ассоциировались с большим числом моторных навыков по сравнению с пациентами с отсутствием реабилитации (рpadj = 0,028).
Сравнительный анализ результатов собственного исследования и данных литературы по эффективности реабилитации при СМА подтверждает полученные нами результаты. В исследовании Г.Н. Пономаренко и соавт. с участием 50 пациентов со СМА 2-го и 3-го типов (средний возраст 7,2 ± 2,4 года) показано, что комплексная медицинская реабилитация, включающая кинезиотерапию, ортезирующие методики и электронейростимуляцию, приводит к улучшению клинического статуса, увеличению подвижности суставов и моторной функции. Использование у пациентов со СМА комплексной медицинской реабилитации показало достаточную статистически значимую (p < 0,05) результативность [19].
В обзоре H.I. Shin показано, что появление патогенетической терапии не отменяет необходимости физической реабилитации, а напротив — требует её как средство поддержания и развития моторных функций. По мнению авторов, реабилитационные вмешательства становятся всё более проактивными с точки зрения увеличения продолжительности жизни и стабилизации состояния заболевания [31]. Y.G. Yi и соавт. подчёркивают, что реабилитационные стратегии, включая позиционирование и фиксацию, стояние с поддержкой, коррекцию деформаций опорно-двигательного аппарата, растяжку, физические упражнения, вспомогательные устройства, лёгочную реабилитацию и лечение дисфагии, могут улучшить двигательную функцию, работоспособность, повседневную активность и качество жизни пациентов со СМА. Это подчёркивает важность начинать эти терапевтические стратегии на более ранних стадиях заболевания [47]. Таким образом, полученные нами данные согласуются с результатами отечественных и зарубежных исследований.
Используемый подход количественной оценки общего числа моторных навыков обеспечил чувствительность анализа (в отличие от анализа смены функционального класса), что делает этот метод предпочтительным. Однако, учитывая невозможность оценки детей в стабильном состоянии, например, стабильно «ходячих» пациентов, анализ необходимо дополнять функциональными моторными шкалами (CHOP INTEND, HINE-2, HFMSE, RULM и др.) и другими методиками. Например, в диссертационной работе И.С. Мальцева, посвящённой медицинской реабилитации пациентов со СМА, предложено использование функционального профиля пациента на основе первичного набора базовых категорий Международной классификации функционирования, ограничений жизнедеятельности и здоровья («ICF Based Documentation Form») для оценки эффективности реабилитации при СМА [42, 48].
Заключение
Систематическая комплексная реабилитация перестала быть паллиативной мерой, превратившись в обязательный компонент лечения, улучшающий эффект фармакотерапии и направленный на максимальную реализацию функционального потенциала пациентов в развитии, поддержании и сохранении моторных навыков у пациентов со СМА. В нашем исследовании показано, что регулярная непрерывная комплексная реабилитация, включающая в себя поддерживающие курсы профессиональной реабилитации на базе медицинских учреждений в совокупности с регулярными поддерживающими занятиями дома (домашняя реабилитация) способствует увеличению объёма моторных навыков. Отсутствие регулярной реабилитации или ограничение её лишь эпизодическими курсами без выполнения индивидуализированной ежедневной домашней программы существенно снижает вероятность достижения клинически значимых улучшений, даже при проведении патогенетической терапии. Количественная оценка моторных навыков оказалась более чувствительной, чем категориальная смена функционального класса, что подчёркивает важность применения точных, числовых показателей для выявления даже умеренного, но клинически значимого прогресса в моторном развитии.
Список литературы
1. D’Amico A., Mercuri E., Tiziano F.D., Bertini E. Spinal muscular atrophy. Orphanet J. Rare Dis. 2011; 6: 71. https://doi.org/10.1186/1750-1172-6-71
2. Lefebvre S., Bürglen L., Reboullet S., Clermont O., Burlet P., Viollet L., et al. Identification and characterization of a spinal muscular atrophy-determining gene. Cell. 1995; 80(1): 155–65. https://doi.org/10.1016/0092-8674(95)90460-3
3. Barois A., Estournet B., Duval-Beaupère G., Bataille J., Leclair-Richard D. Infantile spinal muscular atrophy. Rev. Neurol. (Paris). 1989; 145(4): 299–304. (in French)
4. Клинические рекомендации для взрослых: 5q-ассоциированная спинальная мышечная атрофия. М.; 2024. Режим доступа: https://cr.minzdrav.gov.ru/recomend/780
5. Клинические рекомендации: Проксимальная спинальная мышечная атрофия 5q (у детей). М.; 2023. Режим доступа: https://cr.minzdrav.gov.ru/recomend/593
6. Mercuri E., Finkel R.S., Muntoni F., Wirth B., Montes J., Main M., et al. Diagnosis and management of spinal muscular atrophy: Part 1: Recommendations for diagnosis, rehabilitation, orthopedic and nutritional care. Neuromuscul. Disord. 2018; 28(2): 103–15. https://doi.org/10.1016/j.nmd.2017.11.005
7. Belančić A., Galić V., Lovrić Kojundžić S., Ivanković M., Barišić N., Barišić N., et al. Transforming spinal muscular atrophy: From pivotal trials to real-world evidence and future therapeutic frontiers in types 1 and 2. Biomedicines. 2025; 13(8): 1939. https://doi.org/10.3390/biomedicines13081939
8. Bieniaszewska A., Sobieska M., Gajewska E. Functional and structural changes in patients with spinal muscular atrophy treated in Poland during 12-month follow-up: a prospective cohort study. J. Clin. Med. 2024; 13(14): 4232. https://doi.org/10.3390/jcm13144232
9. Chongmelaxme B., Yodsurang V., Vichayachaipat P., Srimatimanon T., Sanmaneechai O. Gene-based therapy for the treatment of spinal muscular atrophy types 1 and 2: a systematic review and meta-analysis. Gene Ther. 2025; 32(4): 301–30. https://doi.org/10.1038/s41434-024-00503-8
10. Cooper K., Nalbant G., Sutton A., Harnan S., Thokala P., Chilcott J., et al. Systematic review of presymptomatic treatment for spinal muscular atrophy. Int. J. Neonatal. Screen. 2024; 10(3): 56. https://doi.org/10.3390/ijns10030056
11. Coratti G., Cutrona C., Pera M.C., Bovis F., Ponzano M., Chieppa F., et al. Motor function in type 2 and 3 SMA patients treated with Nusinersen: a critical review and meta-analysis. Orphanet J. Rare Dis. 2021; 16(1): 430. https://doi.org/10.1186/s13023-021-02065-z
12. Gavriilaki M., Moschou M., Papaliagkas V., Notas K., Chatzikyriakou E., Papagiannopoulos S., et al. Nusinersen in adults with 5q spinal muscular atrophy: a systematic review and meta-analysis. Neurotherapeutics. 2022; 19(2): 464–75. https://doi.org/10.1007/s13311-022-01200-3
13. Hjartarson H.T., Nathorst-Böös K., Sejersen T. Disease modifying therapies for the management of children with spinal muscular atrophy (5q SMA): an update on the emerging evidence. Drug Des. Devel. Ther. 2022; 16: 1865–83. https://doi.org/10.2147/DDDT.S214174
14. McGrattan K., Walsh K., Mehl L., Kaur S., Dilly K.W. Systematic literature review of the impact of spinal muscular atrophy therapies on bulbar function. J. Neuromuscul. Dis. 2025; 12(2): 195–217. https://doi.org/10.1177/22143602241303373
15. Pera M.C., Coratti G., Pane M., Masson R., Sansone V.A., D’Amico A., et al. Type I spinal muscular atrophy and disease modifying treatments: a nationwide study in children born since 2016. EClinicalMedicine. 2024; 78: 102967. https://doi.org/10.1016/j.eclinm.2024.102967
16. Reilly A., Chehade L., Kothary R. Curing SMA: Are we there yet? Gene Ther. 2023; 30(1-2): 8–17. https://doi.org/10.1038/s41434-022-00349-y
17. Катикова О.Ю. Место реабилитации в ведении детей со спинальной мышечной атрофией. Реабилитология. 2024; 2(2): 227–46. https://doi.org/10.17749/2949-5873/rehabil.2024.18
18. Мальцев И.С., Пономаренко Г.Н., Кольцов А.А. Реабилитационные технологии у пациентов со спинальной мышечной атрофией: наукометрический анализ. Вестник физиотерапии и курортологии. 2022; 28(1): 47–50. https://doi.org/10.37279/2413-1627-2022-28-1-47-50 https://elibrary.ru/wqlfto
19. Пономаренко Г.Н., Мальцев И.С., Кольцов А.А., Шошмин А.В. Медицинская реабилитация пациентов со спинальной мышечной атрофией. Вопросы курортологии, физиотерапии и лечебной физической культуры. 2023; 100(2): 5–14. https://doi.org/10.17116/kurort20231000215 https://elibrary.ru/eoohkr
20. Boulay C., Peltier E., Jouve J.L., Pesenti S. Functional and surgical treatments in patients with spinal muscular atrophy (SMA). Arch. Pediatr. 2020; 27(7S): 7S35–9. https://doi.org/10.1016/S0929-693X(20)30275-X
21. Cunha M.C., Oliveira A.S., Labronici R.H., Gabbai A.A. Spinal muscular atrophy type II (intermediary) and III (Kugelberg-Welander). Evolution of 50 patients with physiotherapy and hydrotherapy in a swimming pool. Arq. Neuropsiquiatr. 1996; 54(3): 402–6. https://doi.org/10.1590/s0004-282x1996000300007
22. Dunaway S., Montes J., McDermott M.P., Martens W., Neisen A., Glanzman A.M., et al. Physical therapy services received by individuals with spinal muscular atrophy (SMA). J. Pediatr. Rehabil. Med. 2016; 9(1): 35–44. https://doi.org/10.3233/PRM-160360
23. Fujak A., Kopschina C., Forst R., Mueller L.A., Forst J. Use of orthoses and orthopaedic technical devices in proximal spinal muscular atrophy. Results of survey in 194 SMA patients. Disabil. Rehabil. Assist. Technol. 2011; 6(4): 305–11. https://doi.org/10.3109/17483107.2010.525292
24. Kelle B., Taş D.A., Kozanoğlu E. Kinesio taping application in a pediatric patient with spinal muscular atrophy. Cukurova Med. J. 2016; 41(2): 386–90. https://doi.org/10.17826/cutf.203634
25. Mercuri E., Pera M.C., Scoto M., Finkel R., Muntoni F. Spinal muscular atrophy – insights and challenges in the treatment era. Nat. Rev. Neurol. 2020; 16(12): 706–15. https://doi.org/10.1038/s41582-020-00413-4
26. Montes J., Garber C.E., Kramer S.S., Montgomery M.J., Dunaway S., Kamil-Rosenberg S., et al. А randomized, controlled clinical trial of exercise in patients with spinal muscular atrophy: methods and baseline characteristics. J. Neuromuscul. Dis. 2014; 1(2): 151–61.
27. Wang C.H., Finkel R.S., Bertini E.S., Schroth M., Simonds A., Wong B., et al. Consensus statement for standard of care in spinal muscular atrophy. J. Child. Neurol. 2007; 22(8): 1027–49. https://doi.org/10.1177/0883073807305788
28. Пономаренко Г.Н., Кольцов А.А., Мальцев И.С. Общие вопросы спинальной мышечной атрофии (научный обзор). Этиология, клинические особенности, подходы в реабилитации и ортопедическом лечении. Физиотерапия, бальнеология и реабилитация. 2021; 20(4): 341–55. https://doi.org/10.17816/rjpbr83799 https://elibrary.ru/uhjvwl
29. Cammarano S., Chirico V.A., Giardulli B., Mazzuoccolo G., Ruosi C., Corrado B. Physical and respiratory rehabilitation in spinal muscular atrophy: a critical narrative review. Appl. Sci. 2025; 15(8): 4398. https://doi.org/10.3390/app15084398
30. Mirea A., Leanca M.C., Onose G., Sporea C., Padure L., Shelby E.S., et al. Physical therapy and nusinersen impact on spinal muscular atrophy rehabilitative outcome. Front. Biosci. (Landmark Ed.). 2022; 27(6): 179. https://doi.org/10.31083/j.fbl2706179
31. Shin H.I. Rehabilitation strategies for patients with spinal muscular atrophy in the era of disease-modifying therapy. Ann. Rehabil. Med. 2024; 48(4): 229–38. https://doi.org/10.5535/arm.240046
32. Pane M., Coratti G., Sansone V.A., Messina S., Bruno C., Catteruccia M., et al. Nusinersen in type 1 spinal muscular atrophy: Twelve-month real-world data. Ann. Neurol. 2019; 86(3): 443–51. https://doi.org/10.1002/ana.25533
33. Coratti G., Bovis F., Pera M.C., Scoto M., Montes J., Pasternak A., et al. Determining minimal clinically important differences in the Hammersmith Functional Motor Scale Expanded for untreated spinal muscular atrophy patients: An international study. Eur. J. Neurol. 2024; 31(8): e16309. https://doi.org/10.1111/ene.16309
34. Dunaway Young S., Montes J., Kramer S.S., Marra J., Salazar R., Cruz R., et al. Six-minute walk test is reliable and valid in spinal muscular atrophy. Muscle Nerve. 2016; 54(5): 836–42. https://doi.org/10.1002/mus.25120
35. Glanzman A.M., McDermott M.P., Montes J., Martens W.B., Flickinger J., Riley S., et al. Validation of the children’s hospital of Philadelphia infant test of neuromuscular disorders (CHOP INTEND). Pediatr. Phys. Ther. 2011; 23(4): 322–6. https://doi.org/10.1097/PEP.0b013e3182351f04
36. Krosschell K.J., Maczulski J.A., Scott C., King W., Hartman J.T., Case L.E., et al. Reliability and validity of the TIMPSI for infants with spinal muscular atrophy type I. Pediatr. Phys. Ther. 2013; 25(2): 140–8; discussion 149. https://doi.org/10.1097/PEP.0b013e31828a205f
37. Pera M.C., Coratti G., Forcina N., Mazzone E.S., Scoto M., Montes J., et al. Content validity and clinical meaningfulness of the HFMSE in spinal muscular atrophy. BMC Neurol. 2017; 17(1): 39. https://doi.org/10.1186/s12883-017-0790-9
38. Trundell D., Le Scouiller S., Gorni K., Seabrook T., Vuillerot C. Validity and reliability of the 32-item motor function measure in 2- to 5-year-olds with neuromuscular disorders and 2- to 25-year-olds with spinal muscular atrophy. Neurol. Ther. 2020; 9(2): 575–84. https://doi.org/10.1007/s40120-020-00206-3
39. Krosschell K.J., Townsend E.L., Kiefer M., Simeone S.D., Zumpf K., Welty L., et al. Natural history of 10-meter walk/run test performance in spinal muscular atrophy: A longitudinal analysis. Neuromuscul. Disord. 2022; 32(2): 125–34. https://doi.org/10.1016/j.nmd.2021.08.010
40. Main M., Kairon H., Mercuri E., Muntoni F. The Hammersmith functional motor scale for children with spinal muscular atrophy: a scale to test ability and monitor progress in children with limited ambulation. Eur. J. Paediatr. Neurol. 2003; 7(4): 155–9. https://doi.org/10.1016/s1090-3798(03)00060-6
41. Trundell D., Le Scouiller S., Le Goff L., Gorni K., Vuillerot C. Assessment of the validity and reliability of the 32-item Motor Function Measure in individuals with Type 2 or non-ambulant Type 3 spinal muscular atrophy. PLoS One. 2020; 15(9): e0238786. https://doi.org/10.1371/journal.pone.0238786
42. Мальцев И.С. Медицинская реабилитация пациентов со спинальной мышечной атрофией: Автореф. дисс. … канд. мед. наук. СПб.; 2022.
43. Папина Ю.О., Мельник Е.А., Белоусова Е.Д., Артемьева С.Б., Монахова А.В., Шидловская О.А. и др. Определение критериев функционального класса у пациентов со спинальной мышечной атрофией 5q. Нервно-мышечные болезни. 2024; 14(4): 58–70. https://doi.org/10.17650/2222-8721-2024-14-4-58-70
44. Erdos J., Wild C. Mid- and long-term (at least 12 months) follow-up of patients with spinal muscular atrophy (SMA) treated with nusinersen, onasemnogene abeparvovec, risdiplam or combination therapies: A systematic review of real-world study data. Eur. J. Paediatr. Neurol. 2022; 39: 1–10. https://doi.org/10.1016/j.ejpn.2022.04.006
45. Giess D., Erdos J., Wild C. An updated systematic review on spinal muscular atrophy patients treated with nusinersen, onasemnogene abeparvovec (at least 24 months), risdiplam (at least 12 months) or combination therapies. Eur. J. Paediatr. Neurol. 2024; 51: 84–92. https://doi.org/10.1016/j.ejpn.2024.06.004
46. Coratti G., Bovis F., Pera M.C., Civitello M., Rohwer A., Salmin F., et al. Long-term natural history in type II and III spinal muscular atrophy: a 4-year international study on the Hammersmith Functional Motor Scale Expanded. Eur. J. Neurol. 2024; 31(12): e16517. https://doi.org/10.1111/ene.16517
47. Yi Y.G., Shin H.I., Jang D.H. Rehabilitation of spinal muscular atrophy: Current consensus and future direction. J. Genet. Med. 2020; 17(2): 55–61. https://doi.org/10.5734/JGM.2020.17.2.55
48. ICF Research Branch. ICF Based Documentation Form; 2016. Available at: https://icf-core-sets.org/en/page1.php
Об авторах
Юлия Олеговна ПапинаРоссия
Врач-невролог отд. детской психоневрологии № 2 НИКИ педиатрии и детской хирургии им. академика Ю.Е. Вельтищева ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 125412, Москва, Россия
e-mail: papina.u@pedklin.ru
Александр Раденкович Стеванович
Россия
Специалист по физической реабилитации, специалист по подбору и адаптации ТСР, НИКИ педиатрии и детской хирургии им. академика Ю.Е. Вельтищева ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 125412, Москва, Россия
e-mail: stevanovich.a@yandex.ru
Евгения Александровна Мельник
Россия
Канд. мед. наук, ведущ. науч. сотр. научно-консультативного отд. МГНЦ им. акад. Н.П. Бочкова, 115522, Москва, Россия; мл. науч. сотр. отд. психоневрологии и эпилептологии НИКИ педиатрии и детской хирургии им. академика Ю.Е. Вельтищева ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 125412, Москва, Россия
e-mail: evmel88@gmail.com
Светлана Брониславовна Артемьева
Россия
Канд. мед. наук, отд. детской психоневрологии № 2 НИКИ педиатрии и детской хирургии им. академика Ю.Е. Вельтищева ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 125412, Москва, Россия
e-mail: artemievasb@gmail.com
Дмитрий Владимирович Влодавец
Россия
Канд. мед. наук, доц., руководитель Российского детского нервно-мышечного центра, ведущ. науч. сотр. отд. психоневрологии и эпилептологии НИКИ педиатрии и детской хирургии им. академика Ю.Е. Вельтищева ФГАОУ ВО РНИМУ им. Н.И. Пирогова Минздрава России, 125412, Москва, Россия
e-mail: mityaus@gmail.com
Рецензия
Для цитирования:
Папина Ю.О., Стеванович А.Р., Мельник Е.А., Артемьева С.Б., Влодавец Д.В. Роль реабилитации в развитии моторных навыков у пациентов со спинальной мышечной атрофией 5q, получающих патогенетическую терапию. Неврологический журнал имени Л.О. Бадаляна. 2025;6(4):209-220. https://doi.org/10.46563/2686-8997-2025-6-4-209-220. EDN: glkqnk
For citation:
Papina Yu.O., Stevanovich A.R., Melnik E.A., Artemyeva S.B., Vlodavets D.V. The role of rehabilitation in the development of motor skills in patients with spinal muscular atrophy 5q receiving pathogenetic therapy. L.O. Badalyan Neurological Journal. 2025;6(4):209-220. (In Russ.) https://doi.org/10.46563/2686-8997-2025-6-4-209-220. EDN: glkqnk
JATS XML




























